C.49
El dolor aparece siempre que cualquier tejido resulta dañado y hace que el individuo reaccione apartando el estímulo doloroso
Estar sentado durante un período prolongado sobre el isquion puede provocar una destrucción tisular debido a la ausencia de flujo sanguíneopor el peso del cuerpo.
Tipos de dolor y sus cualidades
Características del dolor rápido:
«Dolor intenso, dolor punzante, dolor agudo y dolor eléctrico»
- Se siente en 0,1 s
- No se siente en tejidos profundos
- Cuando se clava una aguja en la piel
- Cuando se corta con un cuchillo
- Cuando sufre una quemadura intensa
- En una sacudida eléctrica
- Estímulo mecánico y térmico
Características del dolor lento:
«Dolor lento urente, dolor sordo, dolor pulsátil, dolor nauseoso y dolor crónico»
- Se siente pasado mínimo 1 s
- Sufrimiento casi insoportable
- Ligado a una destrucción tisular
- Prolongado
- En la piel
- Tejido
- Órgano profundo.
- Estímulos dolorosos mecánicos, térmicos y químicos
Receptores para el dolor
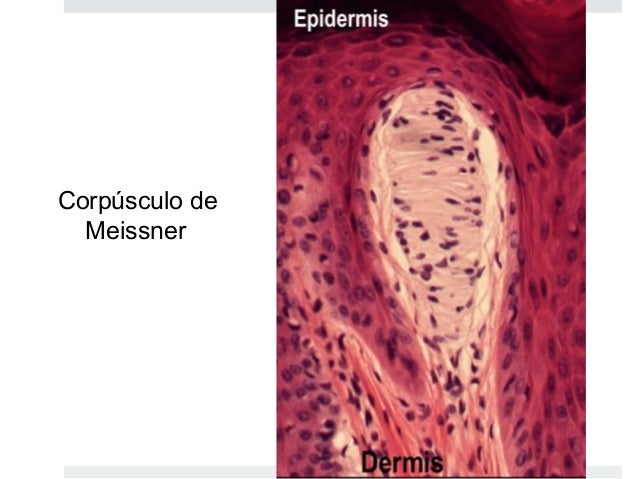
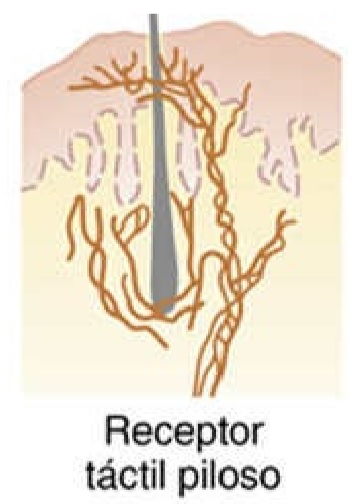
Son terminaciones nerviosas libres que se encuntran en:
- capas superficiales de la piel
- periostio
- paredes arteriales
- superficies articulares
- las hoces y la tienda

En los tejidos profundos se acumula el daño tisular y provoca dolor sordo, crónico y lento.
Dolor Químico
Causado por:
- Bradicinina
- Serotonina
- Histamina
- Iones potasio
- Ácidos, acetilcolina
- Enzimas proteolíticas.
Las prostaglandinas y la sustancia P favorecen la sensibilidad de las terminaciones para el dolor, pero no las activan directamente.
La adaptación de los receptores para el dolor es muy escasa y a veces nula. Es importante porque mantiene informada a la persona que existe un estímulo perjudicial.
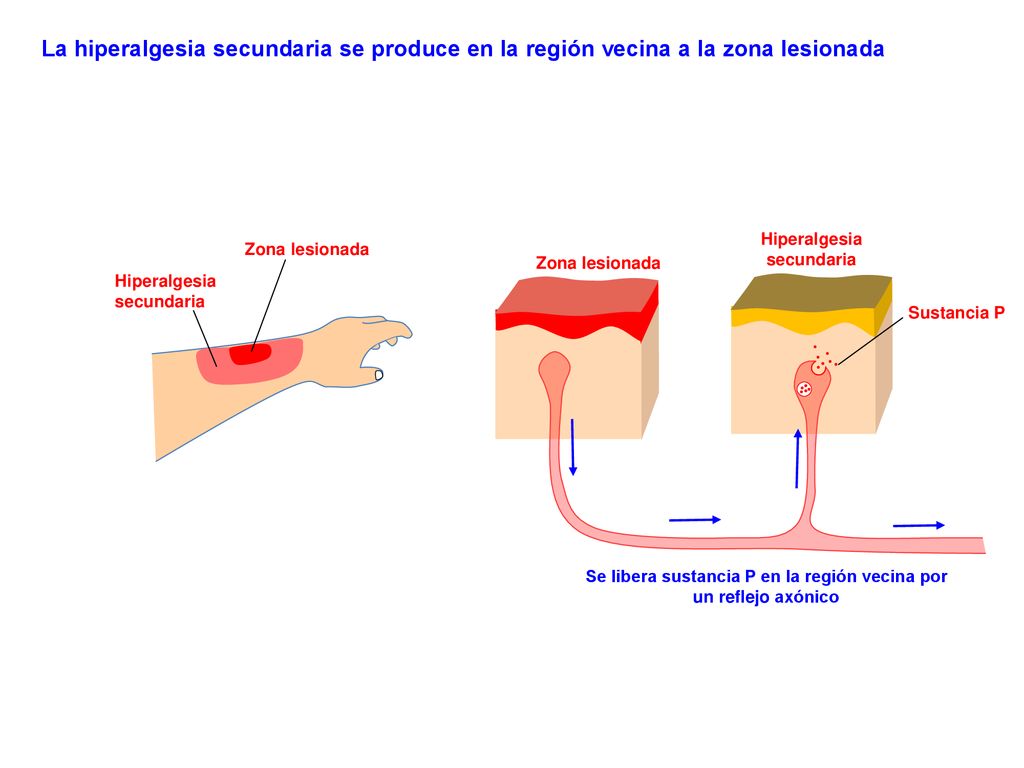
El aumento de la sensibilidad en los receptores para el dolor se llama hiperalgesia.
La piel se calienta por encima de 45 °C y es la temperatura a la que comienzan a dañarse los tejidos por el calor.

La intensidad del dolor está relacionado con la velocidad de la lesión tisular ocasionada por fuentes como:
- Calor
- Infecciones bacterianas
- Isquemia
- Contusión tisular
Una sustancia que parece más dolorosa que las demás es la bradicinina.
Dolor por isquemia
Es la acumulación de grandes cantidades de ácido láctico en los tejidos, debido al metabolismo anaerobio, en los músculos con mayor metabolismo el dolor aparece más rápido.
Espasmo múscular
Es responsable de síndromes clínicos dolorosos que tienen efecto al estimular receptores dolorosos o un efecto indirecto al comprimir vasos sanguíneos causando isquemia, asimismo es capaz de acelerar el metabolismo del tejido.

Vías dobles para la transmisión de las señales de dolor
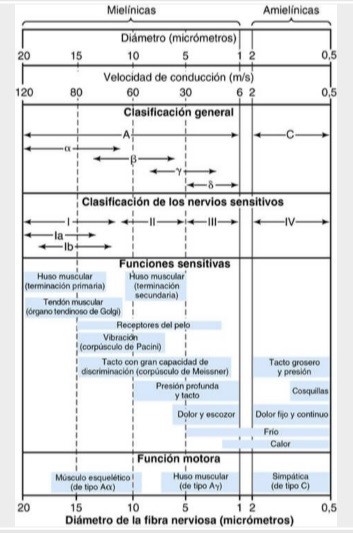
Dolor rápido agudo
- Nace con estímulos dolorosos de tipo mecánico o térmico
- Fibras de tipo Aδ a una velocidad entre 6 y 30 m/s
- Informa la situación lesiva, haciendo que la persona reaccione de inmediato y se aparte del estímulo
- Glutamato
Dolor lento crónico
- Estímulos químicos; estímulos mecánicoso térmicos persistentes
- Fibras de tipo C a una velocidad entre 0,5 y 2 m/s.
- Tiende a crecer con el tiempo causando un dolor intolerable que obliga a la persona a que intente mitigar su causa.
- Sustancia P
- Glutamato actúa de manera inmediata y solo dura unos milisegundos
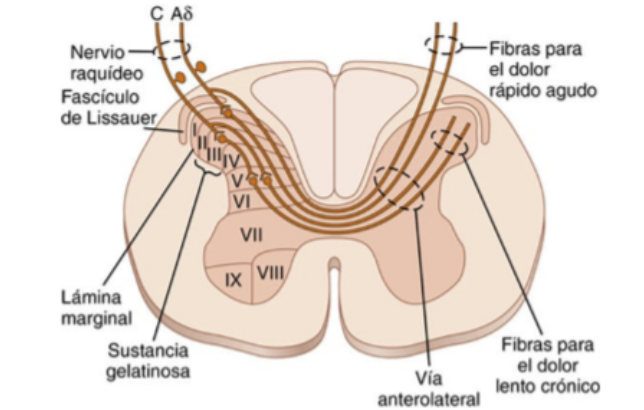
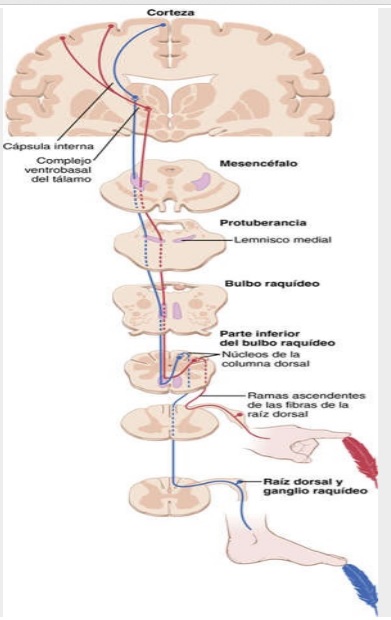
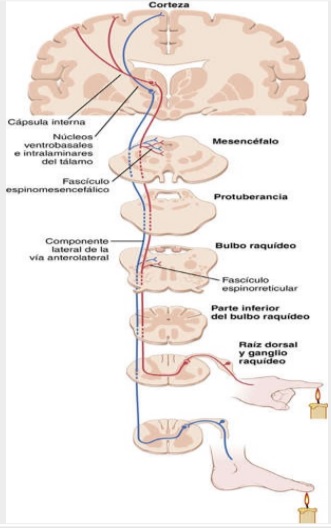
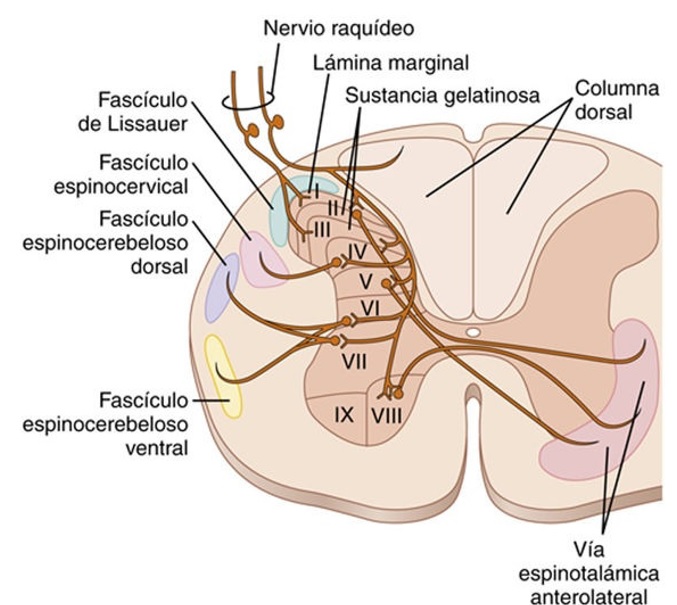
Fascículo neoespinotalámico
- Las fibras de tipo Aδ acaban sobre la lámina I (Lámina marginal) de las astas dorsales donde excitan a las neuronas de segundo orden.
- Las de segundo orden cruzan de inmediato hacia el lado opuesto de la médula y se dirigen al encéfalo por las columnas anterolaterales.
- Terminación en el encéfalo:
- Pocas fibras terminan en la formación reticular.
- La mayoría pasan hacia el tálamo y terminan en el complejo ventrobasal.
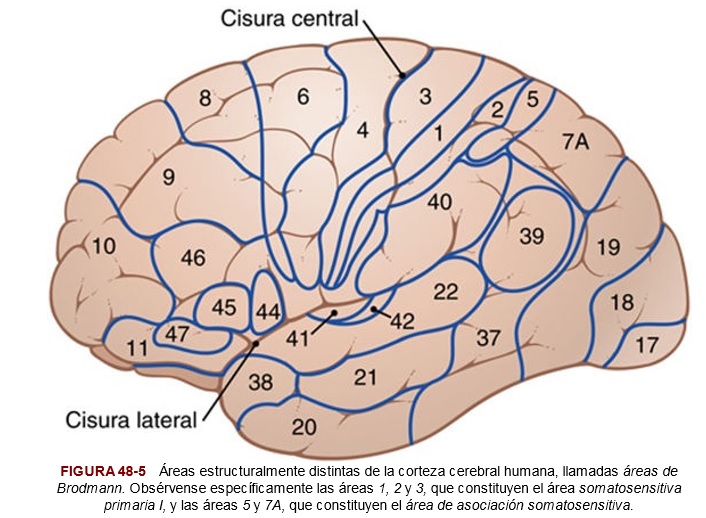
- También en el grupo nuclear posterior del tálamo y se transmiten hacia zonas basales del cerebro o a la corteza somatosensitiva.
- Si la estimulación afecta también a los receptores de la columna dorsal-lemnisco medial, la localización puede ser exacta
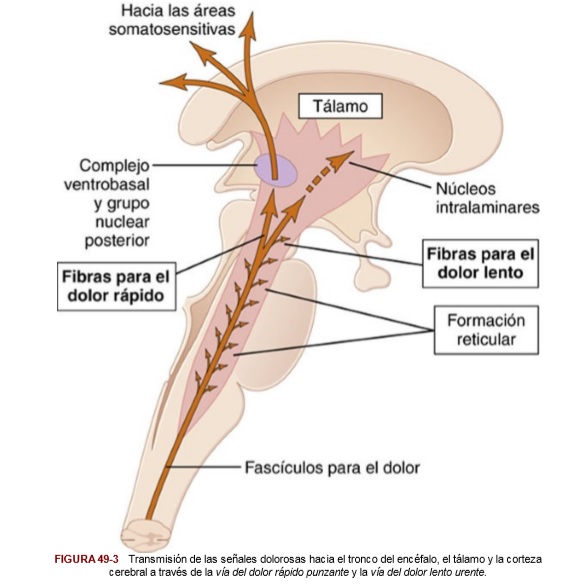
Vía paleoespinotalámica
- Las fibras tipo C terminan entre las láminas II y III de las astas dorsales, que en conjunto reciben el nombre de sustancia gelatinosa

- Las señales atraviesan una o más neuronas complementarias de axón corto dentro de las astas dorsales antes de entrar sobre todo en la lámina V y ascienden por la vía anterolateral.
- Terminación en el encéfalo:
- 1) los núcleos de la formación reticular del bulbo raquídeo, la protuberancia y el mesencéfalo
- 2) la región tectal del mesencéfalo profunda a los colículos superiores e inferiores
- 3) la zona gris periacueductal que rodea al acueducto de Silvio.
- Múltiples neuronas de axón corto transmiten las señales hacia los núcleos intralaminares y ventrolaterales del tálamo y hacia ciertas porciones del hipotálamo.
- La localización es imprecisa, ya que se identifica el dolor en zonas amplias.

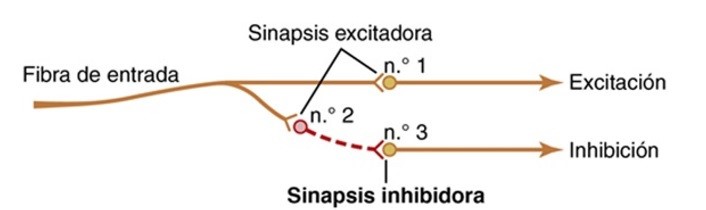
Sistema de supresión de dolor
La variación con la que cada persona siente el dolor obedece a una propiedad que posee el encéfalo para suprimir la entrada de señales dolorosas al sistema nervioso mediante la activación de un mecanismo para controlar el dolor, llamado sistema de analgesia.
Componentes del sistema de analgesia:
- La región gris periacueductal y las áreas periventriculares del mesencéfalo y la parte superior de la protuberancia que rodean al acueducto de Silvio y a las porciones del tercer y del cuarto ventrículos.
- El núcleo magno del rafe, situado en las partes inferior de la protuberancia y superior del bulbo raquídeo, y el núcleo reticular paragigantocelular. A partir de estas estructuras, se transmiten señales descendentes de segundo orden por las columnas dorsolaterales de la médula espinal
- Complejo inhibidor del dolor localizado en las astas dorsales de la médula espinal. A este nivel, las señales analgésicas tienen la capacidad de bloquear el dolor antes de su transmisión hacia el encéfalo.
La serotonina y la encefalina son sustancias que participan en el sistema analgésico.
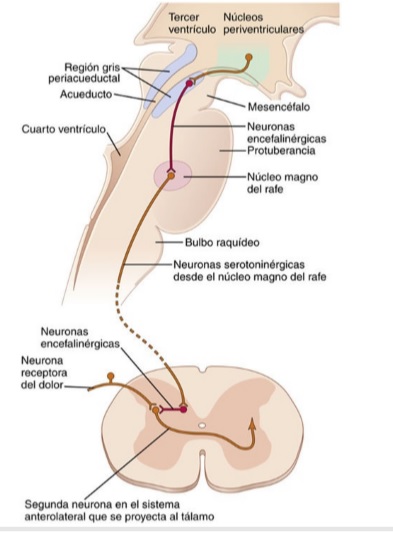
1) Núcleos periventriculares del hipotálamo
2) Fascículo prosencefálico medial
La encefalina propicia una inhibición presináptica y postsináptica de las fibras para el dolor de tipo C y Aδ.
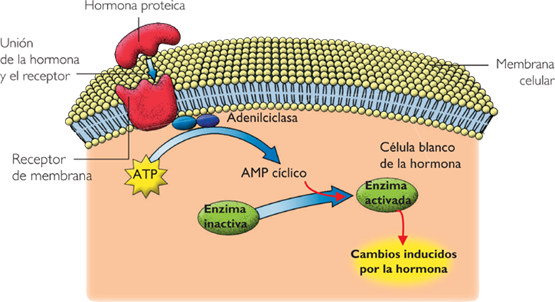
Opioides cerebrales: Endorfinas y Encefalinas
Todos ellos son productos de degradación de tres grandes moléculas proteicas:
- Proopiomelanocortina
- Proencefalina
- Prodinorfina
Entre los más importantes figuran la β-endorfina, la metencefalina, la leuencefalina y la dinorfina.
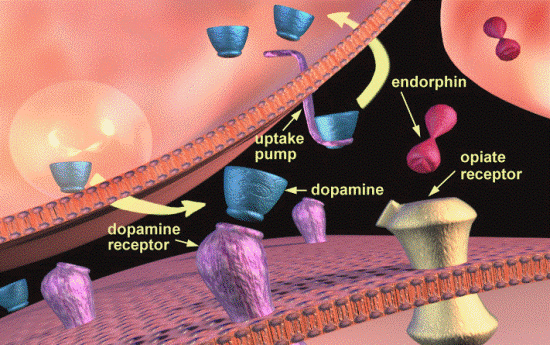
- Las dos encefalinas están presentes en el tronco del encéfalo y en la médula espinal, dentro de las porciones del sistema de analgesia.
- La β-endorfina lo está en el hipotálamo y en la hipófisis.
- La dinorfina se encuentra básicamente en las mismas zonas que las encefalinas, pero en una cantidad mucho menor.
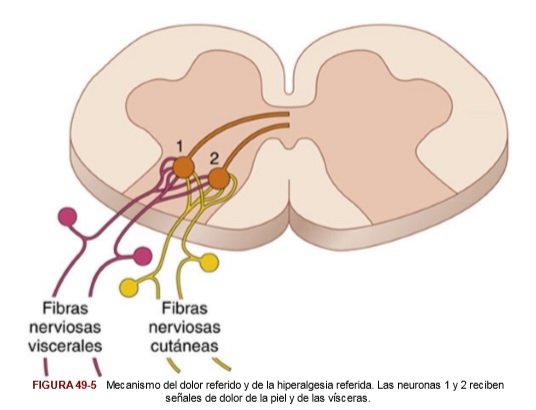
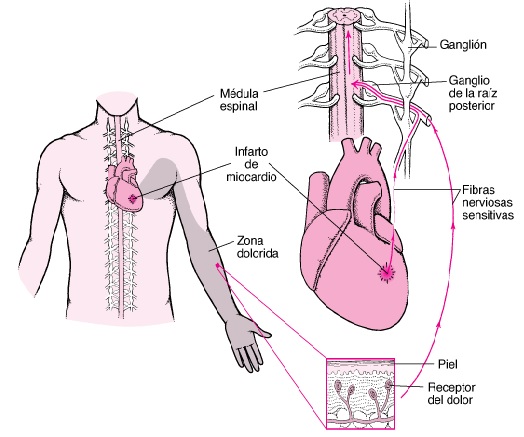
Dolor referido

Es aquel dolor en una parte del cuerpo situada bastante alejada del tejido que lo origina. Se produce porque las fibras para el dolor visceral hacen sinapsis en la médula espinal sobre las mismas neuronas de segundo orden que reciben señales dolorosas desde la piel.
Dolor Visceral
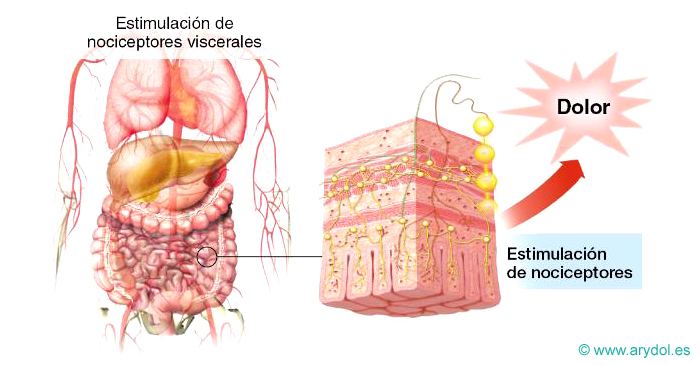
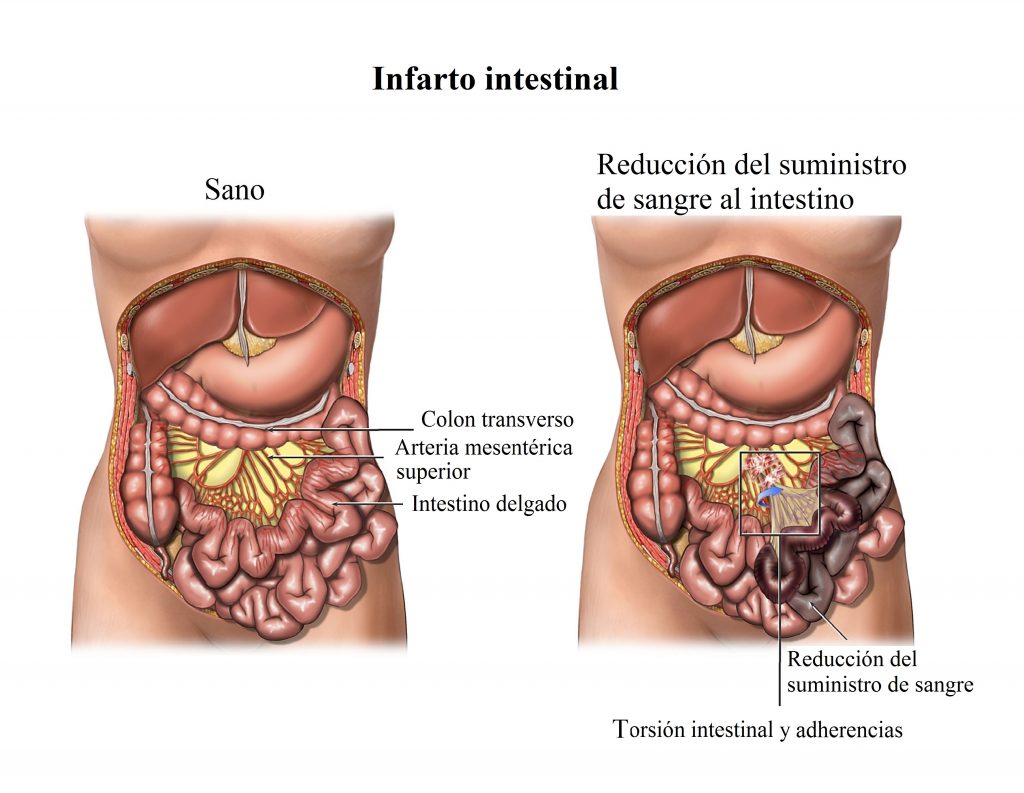
Es un criterio para diagnosticar una inflamación visceral o una enfermedad infecciosa. Y se origina por la isquemia ocasionada por la oclusión del riego sanguíneo en una región intestinal. Se transmite a través de fibras pequeñas para el dolor de tipo C.

Causas del dolor visceral:
Isquemia
Formación de productos finales del metabolismo ácido o de la degeneración tisular, como bradicinina, enzimas proteolíticas.
Estímulos químicos
Se observa desde el tubo digestivo a la cavidad peritoneal. Por ejemplo, el jugo gástrico proteolítico de carácter ácido puede salir a través de una úlcera gástrica o duodenal perforada que produce la digestión del peritoneo causando un dolor terrible.

Espasmo de las vísceras huecas
Se produce debido a la estimulación mecánica de las terminaciones nerviosas, asimismo se puede bloquear el flujo sanguíneo que se dirige al músculo causando dolor por isquemia.

Adopta la forma de cólicos, los cuales suceden de modo intermitente debido a los períodos de contracción del músculo liso.

Cada vez que viaja una onda peristáltica a lo largo de un intestino espástico hiperexcitable, se produce un retortijón. Sucede en personas con apendicitis, gastroenteritis, estreñimiento, menstruación, parto, colecistopatía u obstrucción ureteral.
Hiperdilatación de una víscera hueca
Causa dolor debido a hiperestiramiento de los tejidos y puede colapsar los vasos sanguíneos que rodean la víscera o atraviesan su pared.
Visceras insensibles:
- El parénquima hepático y los alvéolos pulmonares son casi completamente insensibles al dolor de cualquier clase.
>>Dolor parietal<<
Cuando una enfermedad afecta a una víscera, el proceso patológico se propaga al peritoneo parietal, la pleura o el pericardio. Estas superficies, reciben una amplia inervación de los nervios raquídeos periféricos. Por tanto, el dolor de la pared que cubre a una víscera es de carácter agudo.
Razones por las que cuesta localizar el dolor procedente de las vísceras:
- Cerebro no posee experiencia sobre la existencia de órganos internos.
- Las sensaciones se transmiten a través de dos vías hacia el sistema nervioso central:
- Vía visceral verdadera:
- A través de nervios autónomos, causando sensaciones referidas.
- Vía parietal
- Se transportan directamente desde el peritoneo parietal, la pleura o el pericardio hacia los nervios raquídeos locales, y suelen quedar localizadas directamente.
- Vía visceral verdadera:
Dolor referido a través de vías viscerales
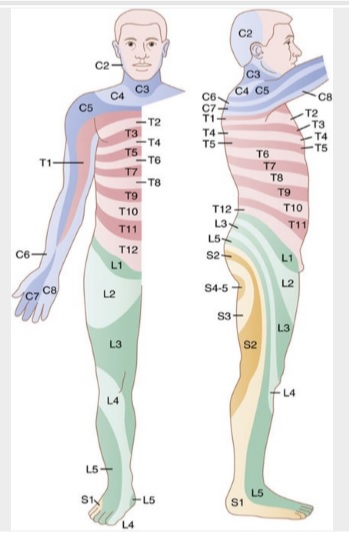
Se localiza en el dermatoma del segmento del que procedía eL órgano visceral en el embrión.
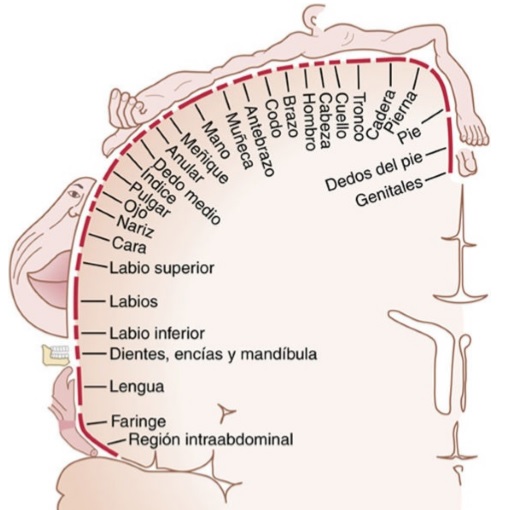
El dolor de origen cardíaco queda referido a la zona lateral del cuello, a la que cubre el hombro, los músculos pectorales, desciende por el brazo y llega al área subesternal de la parte alta del tórax. Envían sus propias fibras nerviosas somatosensitivas hacia los segmentos medulares C3 a T5 (Nervios sensitivos simpáticos).
El estómago presenta su origen aproximado en los segmentos T7 a T9 del embrión. Por tanto, el dolor gástrico queda referido al epigastrio anterior por encima del ombligo.

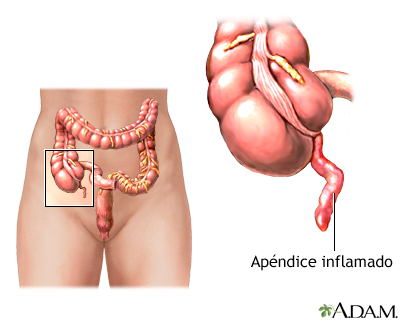
Apendicitis
Los impulsos dolorosos viajan a través de las fibras para el dolor visceral de los haces nerviosos simpáticos y después entran en la médula espinal en torno a T10 o T11; este dolor queda referido a una región que rodea al ombligo y posee una naturaleza fija y cólica.
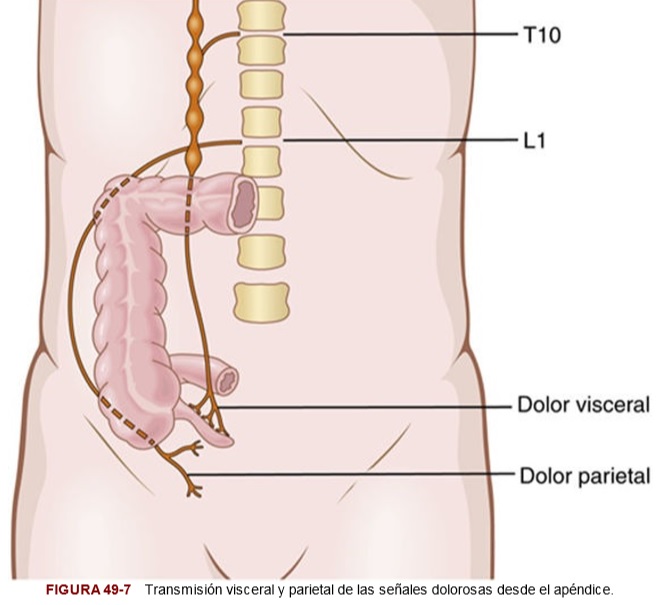
Los impulsos dolorosos también se originan en el peritoneo parietal, donde el apéndice inflamado entra en contacto con la pared abdominal o está adherido a ella. Estos impulsos provocan un dolor de tipo agudo directamente sobre el peritoneo irritado en el cuadrante inferior derecho del abdomen.
Hiperalgesia
Hipersensibilidad al dolor
Se produce cuando una vía nerviosa para el dolor a veces se vuelve demasiado excitable.
Posibles causas:
- Sensibilidad excesiva de los receptores para el dolor (Hiperalgesia primaria)
- Piel quemada por el sol; sensibilización de las terminaciones cutáneas para el dolor por los productos tisulares locales liberados por la quemadura (histamina, prostaglandinas).
2. Facilitación de la transmisión sensitiva (Hiperalgesia secundaria); suele deberse a lesiones en la médula espinal o en el tálamo.
Herpes Zoster
En ocasiones, el virus herpes infecta un ganglio raquídeo generando un intenso dolor en el dermatoma del segmento inervado por ese ganglio, lo que suscita un tipo de dolor segmentario.
El virus se transporta hacia el exterior por el flujo citoplásmico neuronal a través de los axones periféricos hasta su punto de origen cutáneo. Aquí causa un exantema que se vesicula en cuestión de días y después forma costras.

Tic doloroso
Neuralgia del trigémino o del glosofaríngeo.
Es un tipo de dolor lancinante o punzante en un lado de la cara que sigue la zona de distribución sensitiva del quinto o del noveno par. Resulta desencadenado por zonas sensibles en la superficie de la cara, en la boca o en el interior de la garganta (casi siempre por un estímulo mecanorreceptor).

Se alivia mediante la sección quirúrgica del nervio sensitivo periférico procedente de la región hipersensible. Para respetar los componentes motores, necesarios para muchos movimientos mandibulares. En ocasiones fracasa, debido a que la lesión podría estar en el núcleo sensitivo del tronco del encéfalo.
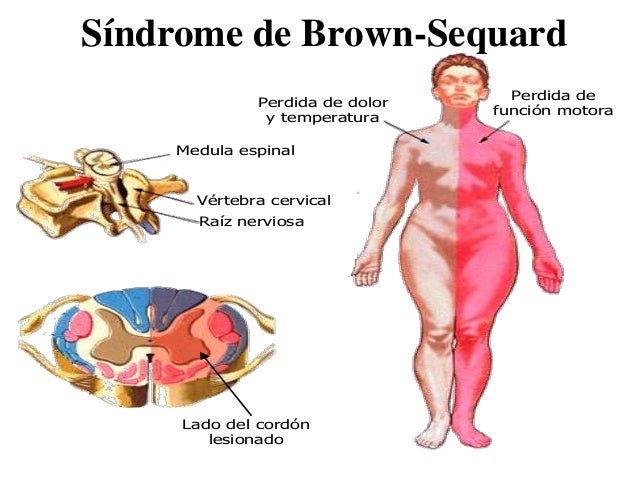
Síndrome de Brown – Séquard
Si la médula espinal sufre una sección completa, todas las sensibilidades y las funciones motoras quedan anuladas, pero si este proceso solo sucede en un lado, aparece el síndrome de Brown-Séquard.
Cefalea
Son un tipo de dolor referido a la superficie de la cabeza desde sus estructuras profundas. Algunas derivan de estímulos dolorosos que nacen en el interior del cráneo, pero otras lo hacen de un dolor cuyo origen está fuera.
Cefalea de origen intracraneal
La estimulación de los receptores para el dolor situados en la bóveda craneal por encima de la tienda, desencadena impulsos dolorosos en la porción cerebral del quinto par.
Los impulsos dolorosos procedentes de la zona infratentorial penetran en el sistema nervioso central a través de los nervios IX, X y segundo cervical, causando una cefalea occipital.
1. Cefalea de la meningitis
Proceso que causa una inflamación de todas las meninges, incluidas las áreas sensibles de la duramadre y las que rodean los senos venosos.

2.Cefalea ocasionada por un descenso en la presión del líquido cefalorraquídeo
La retirada de 20 ml de líquido elimina parte del componente de flotación cerebral, el peso del cerebro estira y deforma las superficies de la duramadre, así desencadena el dolor que causa la cefalea.
3.Jaqueca
“Cefalea migrañosa” puede derivar de fenómenos vasculares anormales. Suelen comenzar con sensaciones prodrómicas, como náuseas, pérdida de la visión, auras visuales y alucinaciones sensitivas. En general, los síntomas prodrómicos empiezan de 30 min a 1 h antes de iniciarse la cefalea.
- Posibles causas:
- Emoción prolongada
- Diseminación de presión cortical
- Alteraciones psicológicas
- Vasoespasmo por exceso de potasio del líquido extracelular
- Predisposición genética (65 a 95 % de los casos)
4.Cefalea alcohólica
Debido a la naturaleza tóxica del alcohol para los tejidos, irrita directamente las meninges y genera el dolor intracraneal, o bien por la deshidratación.
Cefalea de origen extracraneal
1.Cefalea resultante de un espasmo muscular
La tensión emocional hace que muchos de los músculos de la cabeza, sobre todo los que se insertan en el cuero cabelludo y la musculatura cervical, queden espásticos.
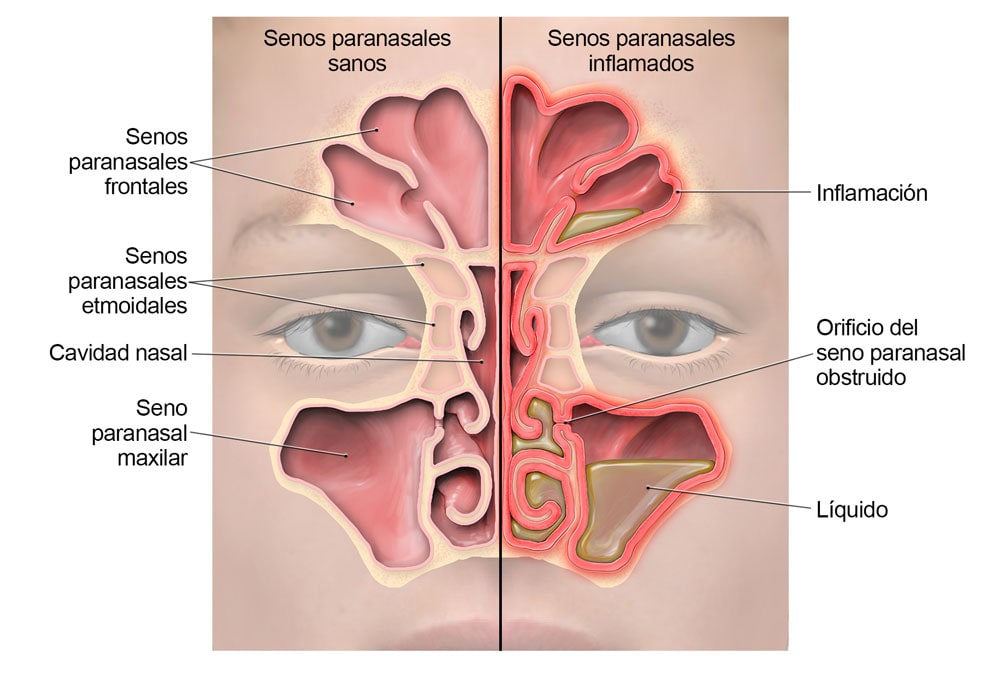
2.Cefalea por irritación de estructuras nasales y paranasales
Una infección o procesos irritantes en regiones de las estructuras nasales propician una cefalea que queda referida detrás de los ojos, a la frente, el cuero cabelludo y cara.
3.Cefalea por trastornos oculares
- Problemas para enfocar la vista. Originan una contracción muy potente de los músculos ciliares cuya contracción tónica puede provocar una cefalea retroorbitaria.
- Irradiación excesiva por los rayos luminosos(UV). Puede surgir una cefalea que dure de 24 a 48h.
- Irritación «actínica» de las conjuntivas. El dolor queda referido a la superficie de la cabeza o a una posición retroorbitaria.

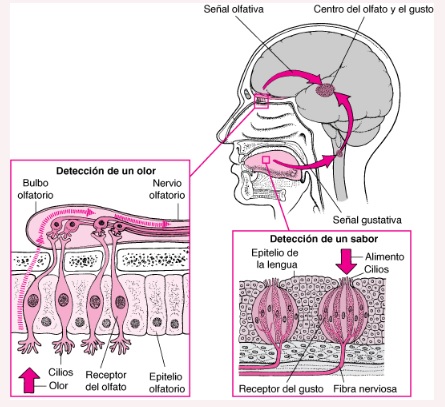
Sensibilidad térmica
Los receptores para el dolor se estimulan únicamente ante un grado extremo de calor o de frío y, por tanto, son responsables de las sensaciones de «frío helado» y «calor ardiente».
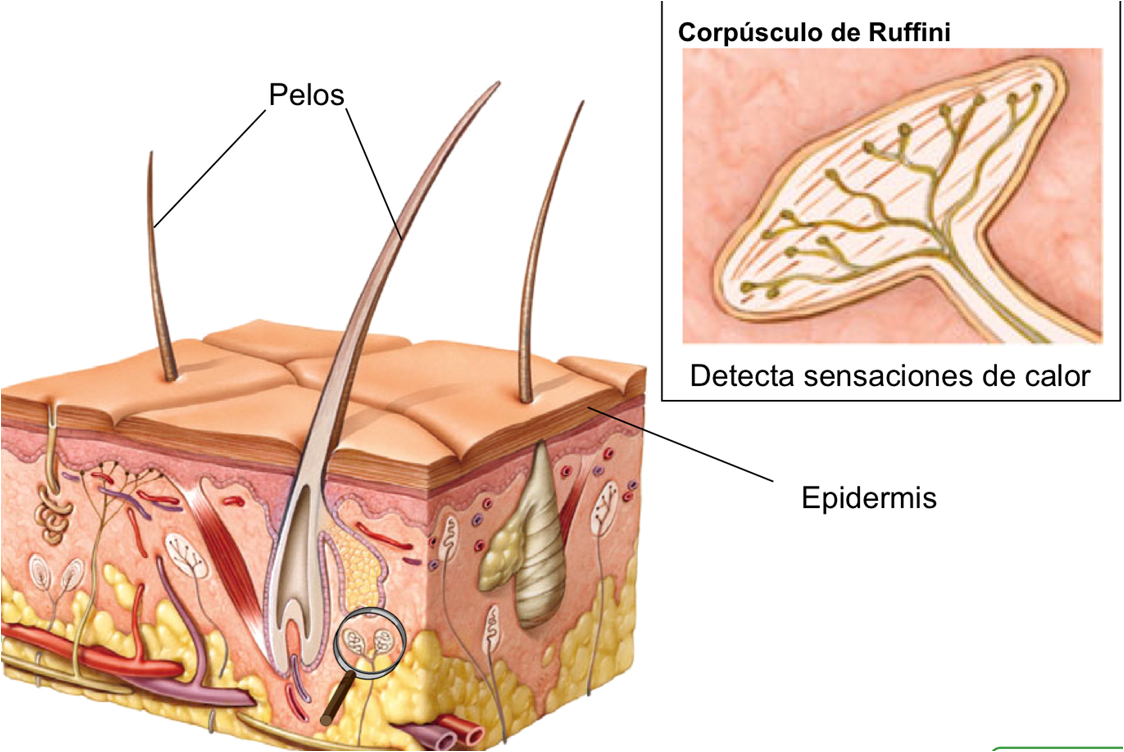
Receptores para el calor son terminaciones nerviosas libres con fibras nerviosas de tipo C.
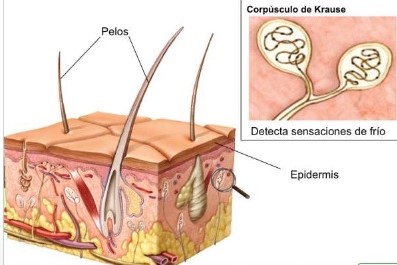
Receptores para el frío son terminaciones nerviosas mielínicas pequeñas de tipo Aδ.
Transmisión de señales térmicas
- Al entrar en la médula espinal, ascienden o descienden unos cuantos segmentos por el fascículo de Lissauer.
- Después terminan sobre todo en las láminas I, II y III de las astas dorsales.
- Las señales se incorporan a fibras ascendentes largas que cruzan hacia el fascículo sensitivo anterolateral opuesto y acaban en:
- 1) la formación reticular del tronco del encéfalo
- 2) el complejo ventrobasal del tálamo.
- 3) Unas pocas también llegan a la corteza sensitiva somática del cerebro desde el complejo ventrobasal.

Una neurona del área sensitiva somática cortical I es sensible directamente a los estímulos de frío o de calor en una zona específica de la piel. En la eliminación de la circunvolución poscentral de la corteza en su integridad va a reducir la capacidad de distinguir gradaciones de temperatura.